Questão 26
Um corpo é abandonado do alto de um plano inclinado, conforme a figura abaixo. Considerando as superfícies polidas ideais, a resistência do ar nula e 10 m/s2 como a aceleração da gravidade local, determine o valor aproximado da velocidade com que o corpo atinge o solo:

A) v = 84 m/s
B) v = 45 m/s
C) v = 25 m/s
D) v = 10 m/s
E) v = 5 m/s
V2 = 100, V = 10.
Questão 27
Em atividades experimentais, usando-se a situação abordada no problema anterior, verifica-se que o valor da velocidade quando o objeto toca o solo é menor do que o valor esperado quando calculado através do teorema da Conservação da Energia Mecânica. Isto é possível pois
A) o problema não apresenta os valores de temperatura e pressão necessários para a utilização do teorema
da Conservação da Energia Mecânica (Não é necessário)
B) para obtermos o valor verdadeiro da velocidade usando o teorema de conservação da energia mecânica, temos que desprezar todo o tipo de forças dissipativas (atrito do corpo com a superfície e atrito do ar). (Errado, se fosse assim só poderíamos calcular a velocidade nestas condições)
C) a grandeza tempo não foi fornecida para o cálculo da velocidade com o teorema da Conservação da Energia Mecânica. (Não é necessário)
D) não foi fornecida a grandeza força necessária para a obtenção da velocidade com o teorema da Conservação da Energia Mecânica. (Não é necessário)
E) a velocidade é uma grandeza vetorial e não pode ser calculada com dados experimentais. (Errado, pode ser calculada por meios experimentais, sim!)
O princípio da conservação da energia mecânica diz que num sistema isolado constituído por corpos que interagem apenas com forças conservativas, a energia mecânica total permanece constante.
Um corpo em queda livre perde constantemente energia potencial gravítica mas, ao mesmo tempo, aumenta a sua velocidade, de forma que aumenta também a sua energia cinética.
No caso de não existirem atritos, a diminuição da energia potencial gravítica em qualquer ponto do percurso é igual ao aumento de energia cinética.
Do mesmo modo, se um corpo for lançado para cima, o aumento da energia potencial gravítica entre dois pontos é igual à diminuição da energia cinética.
Questão 28
O conjunto de valores numéricos que uma dada temperatura pode assumir em um termômetro constitui uma escala termométrica. Atualmente, a escala Celsius é a mais utilizada; nela adotou-se os valores 0 para o ponto de fusão do gelo e 100 para o ponto de ebulição da água. Existem alguns países que usam a escala Fahrenheit, a qual adota 32 e 212 para os respectivos pontos de gelo e de vapor. Certo dia, um jornal europeu informou que, na cidade de Porto Seguro, o serviço de meteorologia anunciou, entre a temperatura máxima e a mínima, uma variação Δ F = 36 ºF. Esta variação de temperatura expressa na escala Celsius é:
A) ΔC = 10 ºC
B) ΔC = 12 ºC
C) ΔC = 15 ºC
D) ΔC = 18 ºC
E) ΔC = 20 ºC

Gabarito: E
Comentários: é só utilizar a fórmula abaixo e achar o resultado. Não esqueça de entrar com a variação da temperatura º F, que será 32 ºF + 36 ºF = 68 º F.
ºC / 5 = (ºF – 32) / 9
°C/ 5 = (68 – 32) / 9
ºC / 5 = (36) / 9
9 ºC = 180
º C = 180/9
º C = 20
Questão 29
Tanto o eco sonoro como a visão são fenômenos explicados pelo estudo de Ondas. Os dois são manifestações de um dos fenômenos ondulatórios abaixo, a
A) difração
B) refração
C) reflexão
D) polarização
E) ressonância
Gabarito: C
Comentários: tanto a visão como o eco sonoro são fenômenos explicados pela reflexão, a luz bate e volta aos olhos para wque se enxergue algo. O eco, é assim também, o som vai, bate, reflete e volta aos ouvidos.
Questão 30
Um disjuntor é um dispositivo eletromecânico destinado a proteger circuitos contra a sobrecarga e o superaquecimento. Pretende-se dimensionar um disjuntor para proteger um ambiente cuja rede elétrica fornece uma tensão de 120 V e possui uma lâmpada de 60 W, um ar condicionado de 1000 W e um computador de 140 W. Este ambiente ficará mais bem protegido, considerando-se a tolerância de 30%, com um disjuntor de:
A) 30 A
B) 22 A
C) 20 A
D) 13 A
E) 10 A
Questão 31
A variação de entalpia de uma reação química, que ocorre à pressão constante, é representada pelo gráfico:

Admitindo que R corresponde aos reagentes, I ao intermediário e P aos produtos, é correto afirmar que
A) a energia de ativação da segunda etapa da reação é maior que a energia de ativação da primeira etapa. (Errado, a energia de ativação é a energia mínima necessária para que a reação aconteça, portanto, ativou, ocorreu a reação, não existem dois momentos)
B) a variação de entalpia da reação é maior que zero. Desta forma, o processo global é endotérmico.
C) a adição de um catalisador aumenta a velocidade da reação, promovendo, também, aumento na variação de entalpia. (Errado, o catalisador acelera sim a velocidade da reação, mas não aumenta a variação de entalpia)
D) o calor de reação independe do estado de agregação dos reagentes e produtos. (Errado)
E) a velocidade da reação depende apenas da concentração do intermediário I. (A velocidade depende do catalisador)
Reações exotérmicas: as que liberam calor para o meio ambiente.
Questão 32
Os compostos cujas estruturas estão representadas aos pares possuem uma ou mais de uma propriedade que os diferenciam.


Acerca das propriedades e da relação de isomeria entre os compostos, é correto afirmar:
A) As cetonas insaturadas (R)-carvona e a (S)- carvona são consideradas isômeros cis-trans.
B) Com base nas estruturas, conclui-se que a combustão completa de 1 mol de ciclopropano libera a mesma quantidade de calor que a combustão completa de 1 mol de propeno. (com certeza não, a ligação dupla é mais difícil de quebrar, portanto, mais energia)
C) O par de isômeros constitucionais apresenta um composto como a imagem do outro, refletida em um espelho.
D) A hidrogenação catalítica do ciclopropeno e do propeno forma o mesmo composto, o propano.
E) Uma mistura equimolar das cetonas (R)-carvona e (S)-carvona é levógira.
Gabarito: D
Comentários: Isomeria é o fenômeno de dois ou mais compostos apresentarem a mesma fórmula molecular (F.M.) e fórmulas estruturais diferentes.
Os compostos com estas características são chamados de isômeros (iso = igual; meros = partes).
Questão 33
Atualmente, o magnésio metálico é obtido após uma sequência de reações químicas que tem como ponto de
partida a transformação do íon magnésio, presente na água do mar, em seu hidróxido. As equações químicas que demonstram as reações de obtenção do magnésio são:
(I) Ca(OH)2(s) + Mg2+ (aq) Mg(OH)2 (s) + Ca2+ (aq)
(II) Mg(OH)2 (s) + 2HCl (g) MgCl2 (s) 2H2O (l)
(III) MgCl2 (s) Mg(s) + Cl2 (g)
A partir das reações representadas e das propriedades dos elementos e substâncias, é correto afirmar:
A) A formação do Mg (s) ocorre com redução do Mg2+ e oxidação do Cl-.Oxidação é o processo químico em que uma substância perde elétrons, partículas elementares de sinal elétrico negativo. O mecanismo inverso, a redução, consiste no ganho de elétrons por um átomo, que os incorpora a sua estrutura interna.
B) O raio do íon Mg2+ é maior que o do íon Ca2+. (errado, o raio atômico cresce de cima para baixo e da direita para a esquerda. portanto, O raio do íon Mg2+ é menor que o do íon Ca2+)
(errado, o raio atômico cresce de cima para baixo e da direita para a esquerda. portanto, O raio do íon Mg2+ é menor que o do íon Ca2+)
C) Na reação global, um mol de HCl(g) é consumido para cada mol de Mg2+ (aq) que reage.(são 2 mols de HCl(g))
D) A substância oxidante na equação (II) é o hidróxido de magnésio.
E) Ao reagirem 7,5 mols de Mg(OH)2 (s) e 10 mols de HCl (g), o reagente em excesso é o ácido.
Gabarito: A
Questão 34

LISBOA,Júlio Cezar Foschini. (Org.) Química Ser Protanista, vol 2. Edições SM: 2010, p. 39.
O comportamento do gás oxigênio com a variação de temperatura descrito no gráfico, bem como o comportamento físico geral dos gases, permitem afirmar corretamente que
A) as forças atrativas se sobrepõem às forças de repulsão entre as moléculas do gás oxigênio com o aumento da temperatura. (Errado, quanto maior a temperatura, maior a força de repulsão entre as moléculas)
B) as colisões entre as moléculas de um gás aumentam de frequência com o aumento de temperatura, à pressão constante, diminuindo a velocidade média das moléculas e reduzindo sua solubilidade em água. (Em parte está correto, mas aumenta a velocidade)
C) a solubilidade de um gás em um líquido depende da energia cinética das moléculas do gás e da pressão exercida sobre o sistema que comporta o soluto gasoso e o solvente líquido.
D) dois reservatórios de água mantidos sob as mesmas condições de limpeza e pressão de 1 atm, localizados na Bahia, a 35º C, e no Paraná, a 20º C, terão a mesma concentração de O2(g) dissolvido na água. (Errado, pelo gráfico se nota que quanto maior a temperatura, menor a solubuilidade)
E) as concentrações de O2(g) dissolvido em amostras de água do mar Báltico e do mar Vermelho independem de suas concentrações salinas, que são 30 g/L e 40 g/L, respectivamente.
Gabarito: C
Questão 35
As substâncias NH3 (amônia) e BF3 (trifluoreto de boro) são gasosas, incolores e de odor característico. O trifluoreto de boro é muito utilizado como catalisador em reações de polimerizações e altamente reativo com a água. Os derivados da amônia são largamente usados como fertilizantes. Do conhecimento das estruturas e das propriedades dos elementos constituintes das substâncias citadas, NH3 e BF3, e sobre o comportamento físico e químico de ambas, é correto afirmar:
A) A amônia e o triflureto de boro são compostos moleculares com geometria molecular piramidal e
trigonal plana, respectivamente.
B) Ao reagir NH3 com o BF3, forma-se um composto iônico com carga negativa sobre o elemento mais
eletronegativo da amônia.
C) A energia de ionização dos elementos N, H, B e F diminui de valor quando é avaliada a partir do elemento de menor número atômico para o elemento de maior número atômico.
D) A adição de NH3 em água forma uma solução não eletrolítica devido ao tipo de ligação química entre o
nitrogênio e o hidrogênio.
E) O trifluoreto de boro está com oito elétrons na camada de valência do átomo central, tornando o boro um bom doador de elétrons.
Gabarito: A
Questão 36
Tuberculose na Mira
A prevenção da tuberculose, sobretudo em crianças portadoras de HIV pode ganhar um novo aliado. Pesquisadores da Universidade Federal de Minas Gerais (UFMG) descreveram como o sistema imune do hospedeiro reconhece a bactéria Mycobacterium avium, do mesmo gênero da M. tuberculosis, e que, pelas semelhanças, serve como modelo para o estudo da infecção. Pelo mecanismo descrito, um receptor específico das células imunes, o TLR9, identifica o DNA do bacilo. “Esse reconhecimento é um importante mecanismo que desencadeia a resposta imunológica”, afirma Sérgio Costa Oliveira, do Departamento de Bioquímica da UFMG [...]. Ao reconhecer o bacilo, as células de defesa são ativadas a liberar citocinas, que são proteínas importantes no mecanismo de destruição do microorganismo.
Adaptado de: Ciência Hoje, nº 283 / julho de 2011, p. 69.
Sobre a tuberculose e outras patologias de interesse epidemiológico, foram feitas as seguintes proposições:
I - No herpes, com o uso de antibióticos específicos, há a diminuição dos sintomas e posterior eliminação do agente etiológico da doença.(Errado, herpes é uma doença virótica, não se trata com antibiótico)
II - A tuberculose , assim como a meningite, é uma doença que pode ser transmitida por secreção salivar, e ambas podem ser prevenidas por imunização ativa.(Correto, podem ser prevenidas por vacina)
III - A utilização de técnicas adequadas de conservação de alimentos diminui as chances de intoxicação botulínica causada pelo Clostridium botulinium.(Correto, o botulismo é causado por uma bactéria que por má conservação do produto se instala)
IV - Na AIDS, a dupla hélice do DNA do vírus desencadeia uma série de reações imunológicas comandadas pelos macrófagos. (A AIDS é uma doença virótica e tem RNA que produz DNA e as reações imunológicas são comandadas por linfócitos e não macrófagos)
Está(ão) correta(s) apenas a(s) afirmativa(s):
A) I e II
B) II e III
C) I e III
D) II e IV
E) III e IV
Gabarito: B
Questão 37
Ataque de tubarão pode ter ocorrido por imprudência do surfista De acordo com informações do Instituto Oceanário de Pernambuco, a localidade da Praia do Pina, onde ocorreu o ataque de um tubarão a um jovem na manhã desta quarta-feira (29), é uma área onde a prática de surf e qualquer outro tipo de esporte náutico é proibida por decreto do governo estadual. Segundo o presidente do Instituto, Alexandre
Carvalho, a área de proibição desse tipo de prática no litoral pernambucano compreende o trecho que vai desde a praia de Zé Pequeno, no Bairro Novo, em Olinda, até a praia do Paiva. O que inclui totalmente a praia do Pina. Alexandre informou ainda que esse período do ano, por ser inverno, é considerado de maior risco. “Há uma maior quantidade de chuvas, baixa salinidade do mar e as águas ficam mais turvas, o que dificulta a visibilidade dos tubarões”, explica. Ele informou ainda que toda a área de proibição possui sinalização e se o banhista insiste em entrar no mar ele deve estar assumindo o risco.
Disponível em: http://ne10.uol.com.br/canal/cotidiano/noticia/2011/06/ 29/ataque-de-tubarao-pode-ter-ocorrido-por-imprudencia-do-surfista- 280172.php. Acesso em: 29/06/2011
Sobre a Biologia dos peixes e aspectos ecológicos da situação descrita, é correto afirmar :
A) Dentre outros fatores, o ataque de tubarões a humanos pode ser explicado pela abundância de alimento disponível na cadeia alimentar desses animais. (Errado, pode ser explicado por pouco alimento na cadeia alimentar do tubarão)
B) Os tubarões são peixes do grupo dos osteíctes, e apresentam opérculo que encobre quatro ou cinco pares de brânquias. (Errado, tubarão é peixe condricties, não apresentando opérculos)
C) Os condríctes apresentam alta concentração de uréia no sangue – uremia fisiológica – que se constitui em um mecanismo de regulação osmótica para animais marinhos.
D) A linha lateral é uma estrutura presente nos peixes, que está diretamente associada aos processos reprodutivos, a exemplo da corte realizada pelos machos para atrair as fêmeas. (Errado, está relacionada a recepção de estímulos, vibrações, capaz de captar mudanças na temperatura da água, localizar obstáculos e alimentos em águas turvas)
E) A prática de banho de mar no fim da tarde e em regiões profundas e distantes da arrebentação da praia dificultam o ataque de tubarões aos banhistas.
Gabarito: C
Questão 38
O fascinante processo de criação da vida O interesse pelo desenvolvimento embrionário é antigo. Em seus estudos anatômicos, Leonardo da Vinci especulou sobre os mistérios da concepção: desenhou um feto dentro do útero e criou esboços de uma possível ligação entre a medula espinhal e os testículos. No século XVII, cientistas naturalistas acreditavam que o espermatozoide abrigaria um bebê em miniatura, pronto para usar o útero como incubadora. Hoje temos ao nosso alcance informações significativas, que esclarecem boa parte das nossas dúvidas. Recursos de ultrassonografia permitem acompanhar a evolução da gravidez desde os primeiros dias após a fecundação, e descobertas no campo da genética trouxeram revelações sobre hereditariedade.
Adaptado de: Mente & Cérebro, nº 222, julho de 2011, p. 12.
Sobre desenvolvimento humano, é correto afirmar que:
A) O ovócito II, durante a penetração do espermatozoide, completa a 2ª divisão meiótica e dá origem a um óvulo e um 2º glóbulo polar.
B) Nos gêmeos monozigóticos, a fecundação se dá com a participação de dois ovócitos e dois espermatozoides que podem dar origem a crianças de sexos diferentes. (Errado, os gêmeos monozigóticos ou univitelinos a fecundação se dá com a partição de um ovócito e um espermatozóide que da origem a crianças sempre de mesmo sexo)
C) No ciclo menstrual, após o pico de LH, a taxa de estrogênio aumenta e a da progesterona diminui, estimulando o aumento dos níveis de FSH. (Progesterona e Estrogênio diminuem)
D) Aproximadamente cinco semanas depois da fecundação, ocorre o processo de nidação, que estimula a produção de FSH. (O termo nidação refere-se ao momento de implantação de um embrião de mamífero na parede uterina que ocorre durante a blástula. Como o processo de deslocamento do embrião das trompas uterinas (onde ocorreu a fertilização) até o útero pode demorar cerca de 4 a 15 dias, então a fixação do embrião ocorrerá nesse intervalo de tempo (4° ao 15° dia após a fertilização).
E) Na gravidez, o útero produz HCG, que contribuirá para suspensão da menstruação e da ovulação.
Gabarito: A
Comentários: HCG (sigla em inglês para Gonadotrofina Coriónica Humana) também é o nome no Brasil do exame para detectar a gravidez.
O embrião, quando atinge o útero, produz um hormônio chamado Hormônio Coriônico Gonadotrófico (HCG). Esse hormônio “manda" o ovário produzir estrogênio e a progesterona.
Esse estrogênio e progesterona chegam à hipófise, "avisando" a hipófise de que a mulher está grávida.
Nesse caso, a hipófise para de produzir os hormônios que iriam estimular o ovário para a ovulação, suspendendo, assim, o ciclo menstrual.
Quando uma mulher está grávida, é o exame desse hormônio que dá certeza da gravidez. Esses exames costumam dar positivo no primeiro dia de falha da menstruação.
Questão 39

Os insetos representam um grupo de artrópodes com incrível diversidade, desde habitat ao comportamento. Dentre os aspectos comportamentais, tem-se grande interesse cientifico tanto pelos chamados insetos sociais como por aqueles que têm relação direta com problemas de saúde pública. Sobre a biologia dos insetos e sua relação com aspectos de saúde pública, é correto afirmar que:
A) Na pediculose do couro cabeludo, a capacidade de voo e saltos dos piolhos contribui para sua grande
incidência na idade escolar. (Piolho não tem asa)
B) Os insetos ametábulos, a exemplo das borboletas e piolhos, apresentam desenvolvimento indireto, sem fase larval. (Insetos ametábolos: o prefixo a designa negação. Portanto, são aqueles que, ao saírem do ovo, já são muito semelhantes a um adulto. Portanto, não passam por estágio larval nem sofrem metamorfose. As borboletas são holometábolos, sofrendo metamorfose completa)
C) No grupo dos insetos, seus representantes sempre apresentarão asas e apêndices locomotores de número variável.(Piolho é inseto e não tem asa)
D) A malária e a febre amarela são doenças infecciosas que apresentam insetos como vetor, e para apenas
uma delas há vacinação disponível. (Correto, a febre amarela tem vacina, e realmente apresentam como vetores mosquitos)
E) O processo de ecdise é raro entre os insetos e, quando ocorre, dificulta o crescimento do exoesqueleto e a reprodução. (A ecdise não é rara entre os insetos e é um processo que facilta o crescimento dos insetos, são as mudas, perdas de exoesqueleto)
Gabarito: D
Questão 40
A dupla hélice
Uma curiosidade: hoje se sabe que Rosalind Franklin realizou as pesquisas básicas (o uso de raio X na observação do DNA) que possibilitaram a proposta da estrutura do DNA.Esse fato é reconhecido por James Watson, em seu livro A dupla hélice – um relato pessoal da descoberta da estrutura do DNA (Lisboa, Gradiva, 1987)[...]. A descoberta da dupla hélice foi repleta de emoções, paixões e intrigas.A disputa e a corrida contra o tempo envolveram três grupos de pesquisadores de DNA: os enfants terribles do laboratório de Cavendish, em Cambridge (James Watson e Francis Crick, que não chegavam a formar uma equipe oficial), o grupo do King’s College, em Londres (Maurice Wilkins e Rosalind Franklin), e o grupo da CalTech, na Califórnia, chefiada por Linus Pauling, naquela época o maior químico do mundo.
Adaptado de: OLIVEIRA, Fátima. Engenharia genética: o sétimo dia da criação. São Paulo: Editora Moderna, 2004, p. 68-70.
A partir de seus conhecimentos de Citogenética, analise as proposições a seguir:
I - Na estrutura do DNA, as duas fitas estão unidas por ligações de hidrogênio (pontes);
II – O RNA, nos eucariotos, é produzido no citoplasma e, posteriormente, migra para o núcleo; (Errado, ele é produzido a partir do DNA no núcleo e depois migra para o citoplasma)
III – O anticódon representa a trinca de bases do RNAm , que orientará a RNAr na síntese proteica; (No tRNA há uma trinca de bases nitrogenadas denominadas anticódon, por meio das quais ele se liga temporariamente ao mRNA no ribossomo, pelas bases complementares (códon).
IV – O código genético humano é degenerado, pois pode apresentar mais de um códon para um mesmo aminoácido. (Correto, ser degenerado significa que Dois ou mais códons podem codificar um mesmo aminoácido, por isso costuma-se dizer que o código genético é degenerado. Existem também alguns códons que não correspondem a aminoácido nenhum. Neste último caso, tratam-se de códons que determinam o término do processo de tradução.)
A alternativa em que todas as proposições estão corretas é :
A) I, II, III e IV
B) I e II
C) II e III
D) III e IV
E) I e IV
Gabarito: E
GABARITO: 26 D 27 nula 28 E 29 C 30 D 31 B 32 D 33 A 34 C 35 A 36 B 37 C 38 A
39 D 40 E
Um corpo é abandonado do alto de um plano inclinado, conforme a figura abaixo. Considerando as superfícies polidas ideais, a resistência do ar nula e 10 m/s2 como a aceleração da gravidade local, determine o valor aproximado da velocidade com que o corpo atinge o solo:
A) v = 84 m/s
B) v = 45 m/s
C) v = 25 m/s
D) v = 10 m/s
E) v = 5 m/s
Gabareito: D
Comentários: o movimento é Movimento Retilíneo Uniformemente Variado (MRUV), portanto vamos utilizar a equação de Torriceli para descobrir a velocidade: V2 = V0 + 2 a d, V2 = 0 + 2 . 10 . 5,V2 = 100, V = 10.
Questão 27
Em atividades experimentais, usando-se a situação abordada no problema anterior, verifica-se que o valor da velocidade quando o objeto toca o solo é menor do que o valor esperado quando calculado através do teorema da Conservação da Energia Mecânica. Isto é possível pois
A) o problema não apresenta os valores de temperatura e pressão necessários para a utilização do teorema
da Conservação da Energia Mecânica (Não é necessário)
B) para obtermos o valor verdadeiro da velocidade usando o teorema de conservação da energia mecânica, temos que desprezar todo o tipo de forças dissipativas (atrito do corpo com a superfície e atrito do ar). (Errado, se fosse assim só poderíamos calcular a velocidade nestas condições)
C) a grandeza tempo não foi fornecida para o cálculo da velocidade com o teorema da Conservação da Energia Mecânica. (Não é necessário)
D) não foi fornecida a grandeza força necessária para a obtenção da velocidade com o teorema da Conservação da Energia Mecânica. (Não é necessário)
E) a velocidade é uma grandeza vetorial e não pode ser calculada com dados experimentais. (Errado, pode ser calculada por meios experimentais, sim!)
Gabarito: anulada
Comentários: O princípio da conservação da energia mecânica diz que num sistema isolado constituído por corpos que interagem apenas com forças conservativas, a energia mecânica total permanece constante.
Um corpo em queda livre perde constantemente energia potencial gravítica mas, ao mesmo tempo, aumenta a sua velocidade, de forma que aumenta também a sua energia cinética.
No caso de não existirem atritos, a diminuição da energia potencial gravítica em qualquer ponto do percurso é igual ao aumento de energia cinética.
Do mesmo modo, se um corpo for lançado para cima, o aumento da energia potencial gravítica entre dois pontos é igual à diminuição da energia cinética.
Grandezas escalares
Grandezas escalares , como o tempo (por exemplo, 5 segundos), ficam perfeitamente definidas quando são especificados o seu módulo (5) e sua unidade de medida (segundo). Estas grandezas físicas (que são completamente definidas quando são especificados o seu módulo e a sua unidade de medida) são denominadas grandezas escalares. Exemplos: Densidade, Pressão, Área, Potência, Energia, Temperatura, Comprimento, Resistência, Massa, Tempo.Grandezas vetoriais
Para serem caracterizadas, necessitam de um número e uma unidade (valor algébrico), direção e sentido. Exemplos: força, aceleração, velocidade, torque, quantidade de movimento, deslocamento, indutância, campo elétrico, campo magnético.Questão 28
O conjunto de valores numéricos que uma dada temperatura pode assumir em um termômetro constitui uma escala termométrica. Atualmente, a escala Celsius é a mais utilizada; nela adotou-se os valores 0 para o ponto de fusão do gelo e 100 para o ponto de ebulição da água. Existem alguns países que usam a escala Fahrenheit, a qual adota 32 e 212 para os respectivos pontos de gelo e de vapor. Certo dia, um jornal europeu informou que, na cidade de Porto Seguro, o serviço de meteorologia anunciou, entre a temperatura máxima e a mínima, uma variação Δ F = 36 ºF. Esta variação de temperatura expressa na escala Celsius é:
A) ΔC = 10 ºC
B) ΔC = 12 ºC
C) ΔC = 15 ºC
D) ΔC = 18 ºC
E) ΔC = 20 ºC
Gabarito: E
Comentários: é só utilizar a fórmula abaixo e achar o resultado. Não esqueça de entrar com a variação da temperatura º F, que será 32 ºF + 36 ºF = 68 º F.
ºC / 5 = (ºF – 32) / 9
°C/ 5 = (68 – 32) / 9
ºC / 5 = (36) / 9
9 ºC = 180
º C = 180/9
º C = 20
Questão 29
Tanto o eco sonoro como a visão são fenômenos explicados pelo estudo de Ondas. Os dois são manifestações de um dos fenômenos ondulatórios abaixo, a
A) difração
B) refração
C) reflexão
D) polarização
E) ressonância
Gabarito: C
Comentários: tanto a visão como o eco sonoro são fenômenos explicados pela reflexão, a luz bate e volta aos olhos para wque se enxergue algo. O eco, é assim também, o som vai, bate, reflete e volta aos ouvidos.
Questão 30
Um disjuntor é um dispositivo eletromecânico destinado a proteger circuitos contra a sobrecarga e o superaquecimento. Pretende-se dimensionar um disjuntor para proteger um ambiente cuja rede elétrica fornece uma tensão de 120 V e possui uma lâmpada de 60 W, um ar condicionado de 1000 W e um computador de 140 W. Este ambiente ficará mais bem protegido, considerando-se a tolerância de 30%, com um disjuntor de:
A) 30 A
B) 22 A
C) 20 A
D) 13 A
E) 10 A
Gabarito: D
Comentários: P = V . i, 1200 = 120 . i, i = 10 A, a corrente total desses 3 aparelhos é 10 A, mas considerando que o problema diz "a tolerância de 30%",deve-se levar em conta mais 30%, ou seja, 3 A, dando um total de 13 A.Questão 31
A variação de entalpia de uma reação química, que ocorre à pressão constante, é representada pelo gráfico:
Admitindo que R corresponde aos reagentes, I ao intermediário e P aos produtos, é correto afirmar que
A) a energia de ativação da segunda etapa da reação é maior que a energia de ativação da primeira etapa. (Errado, a energia de ativação é a energia mínima necessária para que a reação aconteça, portanto, ativou, ocorreu a reação, não existem dois momentos)
B) a variação de entalpia da reação é maior que zero. Desta forma, o processo global é endotérmico.
C) a adição de um catalisador aumenta a velocidade da reação, promovendo, também, aumento na variação de entalpia. (Errado, o catalisador acelera sim a velocidade da reação, mas não aumenta a variação de entalpia)
D) o calor de reação independe do estado de agregação dos reagentes e produtos. (Errado)
E) a velocidade da reação depende apenas da concentração do intermediário I. (A velocidade depende do catalisador)
Gabarito: B
Comentários: geralmente, as reações químicas são acompanhadas pela libertação ou
absorção de calor, em virtude das diferenças de estrutura molecular, e
portanto de energia, entre reagentes e produtos. Por exemplo, se os
produtos de uma reação possuem energia superior à dos reagentes, graças à
respetiva estrutura, é necessário que haja uma absorção de energia para
efetivar a reação.Reações exotérmicas: as que liberam calor para o meio ambiente.
Exemplos
- combustão (queima) do gás butano, C4H10
C4H10(g) + 13/2 O2(g) => 4 CO2(g) + 5H20(g) + calor
- combustão do etanol, C2H60:
C2H60(l) + 3O2(g) => 2 CO2(g) + 3 H2O(g) + calor
Na equação química, o calor é representado junto aos produtos para
significar que foi produzido, isto á, liberado para o ambiente durante a reação.
Reações endotérmicas: as que para ocorrerem retiram calor do
meio ambiente.
Exemplos
- decomposição da água em seus elementos:
H20(l) + calor => H2(g) + 1/2 O2(g)
- fotossíntese:
Na equação química, a energia absorvida á representada junto aos reagentes, significando que foi fornecida pelo ambiente aos reagentes.6 CO2(g) + 6 H20(l) + calor => C6H12O6(aq) + 6 O2(g)
Questão 32
Os compostos cujas estruturas estão representadas aos pares possuem uma ou mais de uma propriedade que os diferenciam.
Acerca das propriedades e da relação de isomeria entre os compostos, é correto afirmar:
A) As cetonas insaturadas (R)-carvona e a (S)- carvona são consideradas isômeros cis-trans.
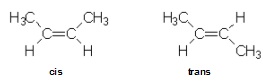
Um composto apresenta isomeria geométrica ou cis-trans quando:
a) tiver dupla ligação carbobo-carbono, e
b) tiver ligantes diferentes a cada carbono da dupla ligação.
Os isômeros cis e trans diferem
pela fórmula espacial. No isômero cis, os ligantes iguais ficam do mesmo
lado do plano da dupla ligação. No isômero trans, os ligantes iguais
ficam em lados opostos ao palno da dupla.
Exemplo:

B) Com base nas estruturas, conclui-se que a combustão completa de 1 mol de ciclopropano libera a mesma quantidade de calor que a combustão completa de 1 mol de propeno. (com certeza não, a ligação dupla é mais difícil de quebrar, portanto, mais energia)
C) O par de isômeros constitucionais apresenta um composto como a imagem do outro, refletida em um espelho.
D) A hidrogenação catalítica do ciclopropeno e do propeno forma o mesmo composto, o propano.
E) Uma mistura equimolar das cetonas (R)-carvona e (S)-carvona é levógira.
Substâncias Dextrogiras
São as substâncias que desviam o plano da luz polarizada para a direita.
São as substâncias que desviam o plano da luz polarizada para a direita.
Substâncias Levógiras
São as substâncias que desviam o plano da luz polarizada para a esquerda.
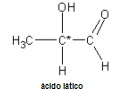
Substâncias com 1 carbono AssimétricoSão as substâncias que desviam o plano da luz polarizada para a esquerda.
Toda substância que apresenta um carbono assimétrico tem dois isômeros espaciais: um dextrógiro e um levógiro.

Gabarito: D
Comentários: Isomeria é o fenômeno de dois ou mais compostos apresentarem a mesma fórmula molecular (F.M.) e fórmulas estruturais diferentes.
Os compostos com estas características são chamados de isômeros (iso = igual; meros = partes).
Questão 33
Atualmente, o magnésio metálico é obtido após uma sequência de reações químicas que tem como ponto de
partida a transformação do íon magnésio, presente na água do mar, em seu hidróxido. As equações químicas que demonstram as reações de obtenção do magnésio são:
(I) Ca(OH)2(s) + Mg2+ (aq)
(II) Mg(OH)2 (s) + 2HCl (g)
(III) MgCl2 (s)
A partir das reações representadas e das propriedades dos elementos e substâncias, é correto afirmar:
A) A formação do Mg (s) ocorre com redução do Mg2+ e oxidação do Cl-.Oxidação é o processo químico em que uma substância perde elétrons, partículas elementares de sinal elétrico negativo. O mecanismo inverso, a redução, consiste no ganho de elétrons por um átomo, que os incorpora a sua estrutura interna.
B) O raio do íon Mg2+ é maior que o do íon Ca2+.
C) Na reação global, um mol de HCl(g) é consumido para cada mol de Mg2+ (aq) que reage.(são 2 mols de HCl(g))
D) A substância oxidante na equação (II) é o hidróxido de magnésio.
E) Ao reagirem 7,5 mols de Mg(OH)2 (s) e 10 mols de HCl (g), o reagente em excesso é o ácido.
Gabarito: A
Questão 34
LISBOA,Júlio Cezar Foschini. (Org.) Química Ser Protanista, vol 2. Edições SM: 2010, p. 39.
O comportamento do gás oxigênio com a variação de temperatura descrito no gráfico, bem como o comportamento físico geral dos gases, permitem afirmar corretamente que
A) as forças atrativas se sobrepõem às forças de repulsão entre as moléculas do gás oxigênio com o aumento da temperatura. (Errado, quanto maior a temperatura, maior a força de repulsão entre as moléculas)
B) as colisões entre as moléculas de um gás aumentam de frequência com o aumento de temperatura, à pressão constante, diminuindo a velocidade média das moléculas e reduzindo sua solubilidade em água. (Em parte está correto, mas aumenta a velocidade)
C) a solubilidade de um gás em um líquido depende da energia cinética das moléculas do gás e da pressão exercida sobre o sistema que comporta o soluto gasoso e o solvente líquido.
D) dois reservatórios de água mantidos sob as mesmas condições de limpeza e pressão de 1 atm, localizados na Bahia, a 35º C, e no Paraná, a 20º C, terão a mesma concentração de O2(g) dissolvido na água. (Errado, pelo gráfico se nota que quanto maior a temperatura, menor a solubuilidade)
E) as concentrações de O2(g) dissolvido em amostras de água do mar Báltico e do mar Vermelho independem de suas concentrações salinas, que são 30 g/L e 40 g/L, respectivamente.
Gabarito: C
Questão 35
As substâncias NH3 (amônia) e BF3 (trifluoreto de boro) são gasosas, incolores e de odor característico. O trifluoreto de boro é muito utilizado como catalisador em reações de polimerizações e altamente reativo com a água. Os derivados da amônia são largamente usados como fertilizantes. Do conhecimento das estruturas e das propriedades dos elementos constituintes das substâncias citadas, NH3 e BF3, e sobre o comportamento físico e químico de ambas, é correto afirmar:
A) A amônia e o triflureto de boro são compostos moleculares com geometria molecular piramidal e
trigonal plana, respectivamente.
B) Ao reagir NH3 com o BF3, forma-se um composto iônico com carga negativa sobre o elemento mais
eletronegativo da amônia.
C) A energia de ionização dos elementos N, H, B e F diminui de valor quando é avaliada a partir do elemento de menor número atômico para o elemento de maior número atômico.
D) A adição de NH3 em água forma uma solução não eletrolítica devido ao tipo de ligação química entre o
nitrogênio e o hidrogênio.
E) O trifluoreto de boro está com oito elétrons na camada de valência do átomo central, tornando o boro um bom doador de elétrons.
Gabarito: A
Questão 36
Tuberculose na Mira
A prevenção da tuberculose, sobretudo em crianças portadoras de HIV pode ganhar um novo aliado. Pesquisadores da Universidade Federal de Minas Gerais (UFMG) descreveram como o sistema imune do hospedeiro reconhece a bactéria Mycobacterium avium, do mesmo gênero da M. tuberculosis, e que, pelas semelhanças, serve como modelo para o estudo da infecção. Pelo mecanismo descrito, um receptor específico das células imunes, o TLR9, identifica o DNA do bacilo. “Esse reconhecimento é um importante mecanismo que desencadeia a resposta imunológica”, afirma Sérgio Costa Oliveira, do Departamento de Bioquímica da UFMG [...]. Ao reconhecer o bacilo, as células de defesa são ativadas a liberar citocinas, que são proteínas importantes no mecanismo de destruição do microorganismo.
Adaptado de: Ciência Hoje, nº 283 / julho de 2011, p. 69.
Sobre a tuberculose e outras patologias de interesse epidemiológico, foram feitas as seguintes proposições:
I - No herpes, com o uso de antibióticos específicos, há a diminuição dos sintomas e posterior eliminação do agente etiológico da doença.(Errado, herpes é uma doença virótica, não se trata com antibiótico)
II - A tuberculose , assim como a meningite, é uma doença que pode ser transmitida por secreção salivar, e ambas podem ser prevenidas por imunização ativa.(Correto, podem ser prevenidas por vacina)
III - A utilização de técnicas adequadas de conservação de alimentos diminui as chances de intoxicação botulínica causada pelo Clostridium botulinium.(Correto, o botulismo é causado por uma bactéria que por má conservação do produto se instala)
IV - Na AIDS, a dupla hélice do DNA do vírus desencadeia uma série de reações imunológicas comandadas pelos macrófagos. (A AIDS é uma doença virótica e tem RNA que produz DNA e as reações imunológicas são comandadas por linfócitos e não macrófagos)
Está(ão) correta(s) apenas a(s) afirmativa(s):
A) I e II
B) II e III
C) I e III
D) II e IV
E) III e IV
Gabarito: B
Questão 37
Ataque de tubarão pode ter ocorrido por imprudência do surfista De acordo com informações do Instituto Oceanário de Pernambuco, a localidade da Praia do Pina, onde ocorreu o ataque de um tubarão a um jovem na manhã desta quarta-feira (29), é uma área onde a prática de surf e qualquer outro tipo de esporte náutico é proibida por decreto do governo estadual. Segundo o presidente do Instituto, Alexandre
Carvalho, a área de proibição desse tipo de prática no litoral pernambucano compreende o trecho que vai desde a praia de Zé Pequeno, no Bairro Novo, em Olinda, até a praia do Paiva. O que inclui totalmente a praia do Pina. Alexandre informou ainda que esse período do ano, por ser inverno, é considerado de maior risco. “Há uma maior quantidade de chuvas, baixa salinidade do mar e as águas ficam mais turvas, o que dificulta a visibilidade dos tubarões”, explica. Ele informou ainda que toda a área de proibição possui sinalização e se o banhista insiste em entrar no mar ele deve estar assumindo o risco.
Disponível em: http://ne10.uol.com.br/canal/cotidiano/noticia/2011/06/ 29/ataque-de-tubarao-pode-ter-ocorrido-por-imprudencia-do-surfista- 280172.php. Acesso em: 29/06/2011
Sobre a Biologia dos peixes e aspectos ecológicos da situação descrita, é correto afirmar :
A) Dentre outros fatores, o ataque de tubarões a humanos pode ser explicado pela abundância de alimento disponível na cadeia alimentar desses animais. (Errado, pode ser explicado por pouco alimento na cadeia alimentar do tubarão)
B) Os tubarões são peixes do grupo dos osteíctes, e apresentam opérculo que encobre quatro ou cinco pares de brânquias. (Errado, tubarão é peixe condricties, não apresentando opérculos)
C) Os condríctes apresentam alta concentração de uréia no sangue – uremia fisiológica – que se constitui em um mecanismo de regulação osmótica para animais marinhos.
D) A linha lateral é uma estrutura presente nos peixes, que está diretamente associada aos processos reprodutivos, a exemplo da corte realizada pelos machos para atrair as fêmeas. (Errado, está relacionada a recepção de estímulos, vibrações, capaz de captar mudanças na temperatura da água, localizar obstáculos e alimentos em águas turvas)
E) A prática de banho de mar no fim da tarde e em regiões profundas e distantes da arrebentação da praia dificultam o ataque de tubarões aos banhistas.
Gabarito: C
Questão 38
O fascinante processo de criação da vida O interesse pelo desenvolvimento embrionário é antigo. Em seus estudos anatômicos, Leonardo da Vinci especulou sobre os mistérios da concepção: desenhou um feto dentro do útero e criou esboços de uma possível ligação entre a medula espinhal e os testículos. No século XVII, cientistas naturalistas acreditavam que o espermatozoide abrigaria um bebê em miniatura, pronto para usar o útero como incubadora. Hoje temos ao nosso alcance informações significativas, que esclarecem boa parte das nossas dúvidas. Recursos de ultrassonografia permitem acompanhar a evolução da gravidez desde os primeiros dias após a fecundação, e descobertas no campo da genética trouxeram revelações sobre hereditariedade.
Adaptado de: Mente & Cérebro, nº 222, julho de 2011, p. 12.
Sobre desenvolvimento humano, é correto afirmar que:
A) O ovócito II, durante a penetração do espermatozoide, completa a 2ª divisão meiótica e dá origem a um óvulo e um 2º glóbulo polar.
B) Nos gêmeos monozigóticos, a fecundação se dá com a participação de dois ovócitos e dois espermatozoides que podem dar origem a crianças de sexos diferentes. (Errado, os gêmeos monozigóticos ou univitelinos a fecundação se dá com a partição de um ovócito e um espermatozóide que da origem a crianças sempre de mesmo sexo)
C) No ciclo menstrual, após o pico de LH, a taxa de estrogênio aumenta e a da progesterona diminui, estimulando o aumento dos níveis de FSH. (Progesterona e Estrogênio diminuem)
D) Aproximadamente cinco semanas depois da fecundação, ocorre o processo de nidação, que estimula a produção de FSH. (O termo nidação refere-se ao momento de implantação de um embrião de mamífero na parede uterina que ocorre durante a blástula. Como o processo de deslocamento do embrião das trompas uterinas (onde ocorreu a fertilização) até o útero pode demorar cerca de 4 a 15 dias, então a fixação do embrião ocorrerá nesse intervalo de tempo (4° ao 15° dia após a fertilização).
E) Na gravidez, o útero produz HCG, que contribuirá para suspensão da menstruação e da ovulação.
Gabarito: A
Comentários: HCG (sigla em inglês para Gonadotrofina Coriónica Humana) também é o nome no Brasil do exame para detectar a gravidez.
O embrião, quando atinge o útero, produz um hormônio chamado Hormônio Coriônico Gonadotrófico (HCG). Esse hormônio “manda" o ovário produzir estrogênio e a progesterona.
Esse estrogênio e progesterona chegam à hipófise, "avisando" a hipófise de que a mulher está grávida.
Nesse caso, a hipófise para de produzir os hormônios que iriam estimular o ovário para a ovulação, suspendendo, assim, o ciclo menstrual.
Quando uma mulher está grávida, é o exame desse hormônio que dá certeza da gravidez. Esses exames costumam dar positivo no primeiro dia de falha da menstruação.
Questão 39
Os insetos representam um grupo de artrópodes com incrível diversidade, desde habitat ao comportamento. Dentre os aspectos comportamentais, tem-se grande interesse cientifico tanto pelos chamados insetos sociais como por aqueles que têm relação direta com problemas de saúde pública. Sobre a biologia dos insetos e sua relação com aspectos de saúde pública, é correto afirmar que:
A) Na pediculose do couro cabeludo, a capacidade de voo e saltos dos piolhos contribui para sua grande
incidência na idade escolar. (Piolho não tem asa)
B) Os insetos ametábulos, a exemplo das borboletas e piolhos, apresentam desenvolvimento indireto, sem fase larval. (Insetos ametábolos: o prefixo a designa negação. Portanto, são aqueles que, ao saírem do ovo, já são muito semelhantes a um adulto. Portanto, não passam por estágio larval nem sofrem metamorfose. As borboletas são holometábolos, sofrendo metamorfose completa)
C) No grupo dos insetos, seus representantes sempre apresentarão asas e apêndices locomotores de número variável.(Piolho é inseto e não tem asa)
D) A malária e a febre amarela são doenças infecciosas que apresentam insetos como vetor, e para apenas
uma delas há vacinação disponível. (Correto, a febre amarela tem vacina, e realmente apresentam como vetores mosquitos)
E) O processo de ecdise é raro entre os insetos e, quando ocorre, dificulta o crescimento do exoesqueleto e a reprodução. (A ecdise não é rara entre os insetos e é um processo que facilta o crescimento dos insetos, são as mudas, perdas de exoesqueleto)
Gabarito: D
Questão 40
A dupla hélice
Uma curiosidade: hoje se sabe que Rosalind Franklin realizou as pesquisas básicas (o uso de raio X na observação do DNA) que possibilitaram a proposta da estrutura do DNA.Esse fato é reconhecido por James Watson, em seu livro A dupla hélice – um relato pessoal da descoberta da estrutura do DNA (Lisboa, Gradiva, 1987)[...]. A descoberta da dupla hélice foi repleta de emoções, paixões e intrigas.A disputa e a corrida contra o tempo envolveram três grupos de pesquisadores de DNA: os enfants terribles do laboratório de Cavendish, em Cambridge (James Watson e Francis Crick, que não chegavam a formar uma equipe oficial), o grupo do King’s College, em Londres (Maurice Wilkins e Rosalind Franklin), e o grupo da CalTech, na Califórnia, chefiada por Linus Pauling, naquela época o maior químico do mundo.
Adaptado de: OLIVEIRA, Fátima. Engenharia genética: o sétimo dia da criação. São Paulo: Editora Moderna, 2004, p. 68-70.
A partir de seus conhecimentos de Citogenética, analise as proposições a seguir:
I - Na estrutura do DNA, as duas fitas estão unidas por ligações de hidrogênio (pontes);
II – O RNA, nos eucariotos, é produzido no citoplasma e, posteriormente, migra para o núcleo; (Errado, ele é produzido a partir do DNA no núcleo e depois migra para o citoplasma)
III – O anticódon representa a trinca de bases do RNAm , que orientará a RNAr na síntese proteica; (No tRNA há uma trinca de bases nitrogenadas denominadas anticódon, por meio das quais ele se liga temporariamente ao mRNA no ribossomo, pelas bases complementares (códon).
IV – O código genético humano é degenerado, pois pode apresentar mais de um códon para um mesmo aminoácido. (Correto, ser degenerado significa que Dois ou mais códons podem codificar um mesmo aminoácido, por isso costuma-se dizer que o código genético é degenerado. Existem também alguns códons que não correspondem a aminoácido nenhum. Neste último caso, tratam-se de códons que determinam o término do processo de tradução.)
A alternativa em que todas as proposições estão corretas é :
A) I, II, III e IV
B) I e II
C) II e III
D) III e IV
E) I e IV
Gabarito: E
GABARITO: 26 D 27 nula 28 E 29 C 30 D 31 B 32 D 33 A 34 C 35 A 36 B 37 C 38 A
39 D 40 E

a resolução da questão 28 está errada
ResponderExcluir